MEDISAN 2026;30e5395
Paciente con virus de inmunodeficiencia humana /SIDA, linfoma no Hodgkin y micobacteriosis atípica
Patient with human immunodeficiency virus HIV / AIDS, non- Hodgkin lymphoma and atypical mycobacteriosis
1Policlínico Universitario Capitán Roberto Fleítes. Villa Clara, Cuba.
2Instituto de Medicina Tropical Pedro Kourí (IPK), La Habana, Cuba.
3Hospital Universitario Arnaldo Milian Castro, Villa clara. Cuba.
Autor para la correspondencia: eltingui97@gmail.com
Recibido: 07/09/2025
Aprobado: 29/01/2026
RESUMEN
En pacientes con VIH, las infecciones por micobacterias atípicas son particularmente graves por la rapidez de la inmunodepresión, de ahí que esta investigación tiene como objetivo ilustrar la complejidad diagnóstica de un caso positivo de VIH, con tratamiento antirretroviral que presentó un linfoma no Hodgkin, generándole una inmunodepresión significativa, que reactivó una micobacteriosis atípica a pesar de ser un paciente con cargas virales y conteos adecuados de linfocitos T CD4 , un desafío para lograr el diagnóstico a pesar del esfuerzo médico que terminó en un desenlace fatal.
ABSTRACT
In HIV-positive patients, infections caused by atypical mycobacteria are particularly serious because of the rapid onset of immunosuppression. Therefore, this reasearch aims at illustrating the diagnostic complexity of an HIV-positive case, with antirretroviral treatment, who developed non-Hodgkin lymphoma, resulting in significant immunosupression that reactivated atypical mycobacteriosis despite the patient having adequate viral loads and CD4 T lymphocyte counts. Diagnosis became a challenge despite medical efforts, ultimately leading to a fatal outcome.
Introducción
La enfermedad avanzada por virus de inmunodeficiencia humana (VIH) es la etapa más grave de la infección por VIH caracterizada por una inmunosupresión marcada y la presencia o riesgo elevado de enfermedades oportunistas entre ellas las micobacteriosis atípicas y neoplasias definitorias de SIDA como el linfoma.^(1)^
Las micobacterias no tuberculosas (MNT), también conocidas como micobacterias atípicas, constituyen un grupo heterogéneo de más de 150 especies de microorganismos ampliamente distribuidos en el ambiente, en medios como el agua, suelo y animales^(2)^ a diferencia del Mycobacterium tuberculosis, su relación con la patología humana es oportunista y ocasional, siendo la mayoría de las especies no patógenas para el ser humano. Sin embargo, en las últimas décadas, las infecciones por MNT han ganado notoriedad clínica, especialmente en pacientes con inmunosupresión subyacente, donde pueden causar enfermedad significativa y de difícil tratamiento.^(3)^
La coexistencia de virus de la inmunodeficiencia humana (VIH) y linfoma no Hodgkin difuso de células B grandes (LNDCGB) crea un estado de inmunosupresión profundamente sinérgico, donde las disfunciones inmunitarias humorales y celulares se potencian, y facilita la aparición de infecciones oportunistas complejas.^(4)^
La intersección clínica entre la infección por VIH, el LNDCGB y las micobacteriosis atípicas representa un desafío diagnóstico y terapéutico de primera magnitud, el diagnóstico de las micobacteriosis atípicas en este contexto es complejo debido a la superposición de síntomas constitucionales entre la infección micobacteriana, el linfoma subyacente y la propia infección por VIH.^(5)^
Esta investigación tiene como objetivo ilustrar la complejidad diagnóstica de un caso positivo a VIH, con tratamiento antirretroviral que desarrolló un linfoma no Hodgkin que generó una inmunodepresión significativa que reactivó la micobacteriosis atípica a pesar de ser un paciente con cargas virales y conteos de linfocitos T CD4 adecuados, se volvió un desafío lograr el diagnóstico a pesar del esfuerzo médico que terminó en un desenlace fatal.
Caso clínico
Se describe el caso de un paciente masculino de 39 años de edad, mestizo, natural del municipio Playa de la Ciudad Habana, graduado de Ingeniero electrónico siendo esta su ocupación actual, no refiere alergias a medicamentos, operaciones o traumas anteriores.
Dentro de sus antecedentes patológicos personales presentó el diagnóstico de VIH desde hace 17 años para lo cual se le prescribió tratamiento con Tenofovir disoproxil fumarate (300 miligramos(mg)/Lamivudina (300 mg)/Dolutegravir 50 mg (TLD)1 tableta vía oral al día, además de diagnóstico de Micobacteriosis atípica en el 2017 por lo cual no mérito tratamiento en esa ocasión y un año después en el 2018 se diagnosticó tuberculosis pulmonar y se indicó tratamiento 2 meses con rifampicina 600 mg/día vía oral al día, isoniacida 300 mg vía oral al día, etambutol 1200 mg/día y pirazinamida 1200 mg/día vía oral y luego 4 meses con rifampicina 600 mg/día vía oral al día, isoniacida 300 mg vía oral al día
Enfermedad actual: refiere el comienzo de fiebre de 38 grados celsius hace 5 meses, con una curva térmica recurrente y frecuencia de 3 a 4 picos por semana, pérdida de peso no cuantificada, astenia, dolor abdominal de carácter difuso que apareció a las 2 semanas de comenzar el cuadro febril, localizado principalmente en epigastrio e hipocondrio derecho, con una escala de dolor referida del 1 al 10 tomando el 10 como máximo dolor en 6, constante que aliviaba con el uso de analgésicos y coincidía con su uso para la fiebre, también refiere el aumento de volumen de adenopatías en la región del cuello, axilar e inguinal.
El cuadro anterior se mantuvo hasta un mes, que cambió en cuanto a la curva térmica febril y la intensidad llegando a ser continúa de 39.5 grados Celsius por lo que acude a su área de salud donde fue valorado y se decide su remisión al IPK para examinarlo y se decide su ingreso.
Examen Físico: Se constata piel y mucosas hipocoloreadas además de la presencia de adenopatías laxas de bordes lisos, sin adherencia a planos profundos, no dolorosas a la palpación en las cadenas ganglionares cervicales anteriores, posteriores submandibulares, axilares e inguinales superficiales.
Frecuencia respiratoria en 19 por minuto, tensión arterial 120/70 milímetros de mercurio, frecuencia cardíaca 105 latidos por minuto.
En los miembros inferiores el tejido celular subcutáneo se encontró infiltrado con edemas fríos de fácil palpación que llegan hasta el nivel de la rodilla, abdomen ligeramente distendido con dolor a la palpación superficial y profunda en todo el abdomen y hepatomegalia dolorosa de 4-5 cm por debajo de reborde costal con esplenomegalia ligera.
Complementarios: según resultados los exámenes presentaron alteraciones, la tomografía axial computarizada de tórax con adenomegalias hilares derechas y adenomegalias mediastinales que mostraron adenopatías y ensanchamiento del mediastino, ferritina 1890 µg/ proteína C reactiva 257 mg/L, hemoglobina 75 g/L, albumina 27.5 g/L, proteínas totales 52 g/L, leucocitos 2.5 x 10^9^ a predominio de linfocitos y plaquetas 25x10^9^, los demás exámenes sin alteraciones.
Evolución: Durante su ingreso la evolución no fue óptima continuó la pérdida de peso, astenia y anorexia, decidiéndose comenzar empíricamente con tratamiento para toxoplasmosis diseminada con Pirimetamina(25mg) 2 tabletas al día y Sulfadiazina (1 gramo)1 ámpula endovenosa cada 6 horas que se cumple durante 10 días, teniendo en cuenta que no se logró evidenciar una respuesta terapéutica adecuada, se decide discutir el caso en el colectivo de la especialidad, donde se emitieron diferentes criterios relacionados con otras infecciones oportunistas entre las que se encuentra la histoplasmosis diseminada que justifica por clínica sugestiva esta patología y se inicia tratamiento con Anfotericina B Liposomal (50mg) a 5 mg/kg/día, una prueba terapéutica con mejoría parcial del patrón febril en cuanto a frecuencia e intensidad.
Después de varias semanas comienza tos con expectoración verdosa, dolor en punta de costado, crepitantes en base derecha, por lo que se indican complementarios que demostraron una anemia marcada, síndrome hemofagocítico y neumonía nosocomial y se comenzó el tratamiento con Piperacilina/tazobactan (4.5 gramos) 1 bulbo endovenoso cada 6 horas y es transfundido con 2 unidades de glóbulos rojos en tres ocasiones.
Luego de algunos días de evolución favorable comenzó con un deterioro clínico significativo resultando positivo al examen físico:
Sistema respiratorio: se presentó disminución de la expansibilidad del hemitórax derecho, matidez hacia esa base pulmonar y en la auscultación crepitantes en bases pulmonares, frecuencia respiratoria de 22 por minuto.
Sistema cardiovascular: frecuencia cardíaca de 124 latidos por minuto.
Sistema Digestivo: abdomen distendido doloroso en flanco derecho y región periumbilical, de gran intensidad que a la palpación superficial y profunda se aumentaba, maniobra de tarral positiva, se comenzó tratamiento con claritromicina (500 mg) 1 tableta cada 12h por vía oral, ceftriaxona endovenoso (1g) 2 bulbos al día.
Se le dio ingreso en la unidad de atención al grave donde se le realiza un hemograma y hemogasometría de urgencia y se detectó plaquetopenia intensa y anemia severa, PH 7.22, PO2 139, PCO21.8, BE 17.2 los demás parámetros normales.
A partir de este momento se sospecha un sangramiento digestivo alto, que es valorado por un especialista en cirugía general sugiriendo endoscopia, antibióticos de amplio espectro y que en esos momentos por el estado de gravedad del paciente la opción quirúrgica resulta imposible, se añadió al tratamiento ácido tranexámico (500mg) 1 ámpula endovenosa cada 8 horas, sonda nasogástrica, que al aspirar se constata contenido que indicó sangre digerida y se comienza terapia con Omeprazol(40mg) 2 bulbos endovenosos en ese momento y luego 1 cada 12 horas además una unidad de plasma fresco y cuatro de plaquetas.
Al día siguiente, se identifica aumento de las enzimas hepáticas en los exámenes complementarios con patrón hepatocelular y se suspende Amfotericina B liposomal. Se realizan cambios en la terapéutica comenzando con meropenem(1gramo) 1 bulbo cada 8h en infusión extendida más clindamicina (600 mg) 1 ámpula cada 6 horas endovenosa. Luego presentó un cuadro clínico de disminución del estado de conciencia con sudoración profusa se evidencia hipoglucemia además de letargia tendencia a la hipotensión arterial y sin respuesta a la terapéutica empleada, se intensificó el cuadro clínico con deterioro de su estado general, hasta llegar a la parada cardiorrespiratoria momento en que se le realizaron maniobras de reanimación sin respuesta y se declara fallecido.
Después de lo anteriormente expuesto y la confirmación por necropsia se plantean los siguientes diagnósticos:
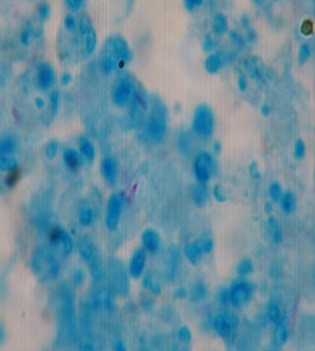
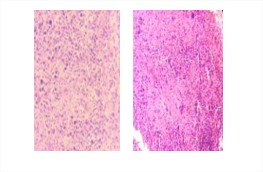
Causa directa de muerte: Disfunción multiorgánica secundaria a sepsis por micobacteriosis atípica diseminada. Z-Nielsen (figura 1), se observan bacilos acidorresistentes (BAAR) en hígado, médula ósea, ganglios linfáticos y bazo, (figura 2).
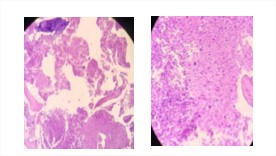
Causa intermedia muerte: Infiltración tumoral de linfoma no Hodgkin difuso de células grandes a hígado, bazo, páncreas, pulmón y médula ósea, (figura 3 y 4).
Causa básica de muerte: VIH/Sida.

Discusión
El diagnóstico de VIH/SIDA en su etapa avanzada se establece no solo por la infección crónica Viral, si no por la presencia de enfermedades indicadoras de inmunodepresión profunda, recuentos de linfocitos T CD4 inferiores a 200 células/µL o la aparición de afecciones oportunistas específicas, según los criterios de los CDC y la OMS.^(1)^
En este contexto la incidencia de neoplasias hematológicas, particularmente el linfoma no Hodgkin difuso de células B grandes (LNDCGB), aumenta de manera significativa, constituyendo una de las principales causas de morbimortalidad y manifestaciones directas de la desregulación inmune, marcando una aceleración en el deterioro inmunológico.^(4)^
Las MNT son patógenos oportunistas cuya importancia clínica ha aumentado significativamente en las últimas décadas, particularmente en pacientes con afección inmunológico. El riesgo de infección diseminada por MNT aumenta dramáticamente cuando los recuentos de linfocitos T CD4+ descienden por debajo de 50 células/μL.^(6)^
La patogénesis de las micobacteriosis atípicas en pacientes con VIH y LNDCGB es compleja y multifactorial. La infección por VIH causa depleción progresiva de linfocitos T CD4+, cruciales para la inmunidad mediada por células contra micobacterias.^(5)^ Por otro lado, el LNDCGB per se causa disfunción inmune tanto humoral como celular, creando un estado de inmunodeficiencia adicional.^(4)^
El diagnóstico de micobacteriosis atípica en pacientes con VIH y LNDCGB presenta desafíos únicos debido a la superposición de síntomas constitucionales entre estas condiciones. Las manifestaciones clínicas suelen ser inespecíficas: fiebre (presente en 96,7% de los casos, pérdida de peso, astenia y sudoración nocturna, que pueden atribuirse erróneamente solo al linfoma o a la infección por VIH.^(7)^
La confirmación microbiológica requiere el aislamiento e identificación de la MNT en muestras clínicas. Las muestras respiratorias (esputo, lavado broncoalveolar) son las más comúnmente positivas.^(8)^
La biopsia tisular con estudio histopatológico e inmunohistoquímico es crucial para diferenciar entre infiltración por linfoma e infección micobacteriana. El pronóstico de los pacientes con VIH, LNDCGB y micobacteriosis atípica depende de múltiples factores. Los indicadores de mal pronóstico incluyen recuentos de linfocitos T CD4+ <50 células/μL, niveles de albúmina <2,5g/dL y pancitopenia, desafortunadamente, el diagnóstico a menudo se retrasa debido a la superposición sintomática entre condiciones y al tiempo requerido para el aislamiento e identificación de las MNT.^(9)^
A modo de conclusión este caso subraya la complejidad del tratamiento en pacientes con infección por VIH, incluso bajo adecuado control virológico, cuando se desarrollan neoplasias asociadas al SIDA, la presentación clínica inespecífica plantea un formidable desafío diagnóstico debido a la superposición de síntomas entre la tríada VIH-linfoma-MNT.
La evolución fatal muestra la naturaleza sinérgica acelerada de la inmunodepresión donde el linfoma no solo es una consecuencia si no un potente inductor del deterioro inmune acelerado que permite la reactivación de la MNT. Además, la confirmación patológica post mortem fue fundamental para establecer los diagnósticos definitivos que exponen el escenario de alta complejidad y la necesidad de integración temprana de un enfoque multidisciplinario.
Referencias bibliográficas
- Organización Mundial de la Salud. Estrategias mundiales del sector de la salud contra el VIH, las hepatitis víricas y las infecciones de transmisión sexual para el periodo 2022-2030. Ginebra: Organización Mundial de la Salud; 2025 [citado 29/01/2026]: 136. Disponible en: https://iris.who.int/server/api/core/bitstreams/efaf3bab-4386-4104-8e69-1a8b8ee052cc/content
- Rozas CF, Cifuentes MM, Flores K, Salinas P D, Troncoso A T, Saldías P F. Caracterización clínica y microbiológica de pacientes no VIH con micobacteriosis atípica pulmonar: experiencia de un centro público. Rev Chil Enferm Respir. 2024[citado 29/01/2026];40(2):118-28. Disponible en: https://revchilenfermrespir.cl/index.php/RChER/article/view/1207/1986
- Esteban J, Navas E. Tratamiento de las infecciones producidas por micobacterias no tuberculosas. Enferm Infecc Microbiol Clin. 2018[citado 29/01/2026];36(9):586-92. Disponible en: https://www.elsevier.es/es-revista-enfermedades-infecciosas-microbiologia-clinica-28-pdf-S0213005X17303026
- Vivas Arteaga JS. Linfoma difuso de células B grandes (LDCBG): epidemiología, clasificación, pronóstico y tratamiento. NPunto. 2025[citado 29/01/2026];8(92):3-4. Disponible en: https://www.npunto.es/revista/92/linfoma-difuso-de-celulas-b-grandes-ldcbg-epidemiologia-clasificacion-pronostico-y-tratamiento
- Hübel K. The changing landscape of lymphoma associated with HIV infection. Current Oncology Reports. 2020[citado 19/10/2025];22(11):111. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC8302507/pdf/11912_2020_Article_973.pdf
- Lange CH, Bothamley G, Günther G, Guglielmetti L, Kontsevaya I , Kuksa L, et al. A Year in Review on Tuberculosis and Non-tuberculous Mycobacteria Disease: A 2025 Update for Clinicians and Scientists. Pathogens and Immunity. 2024[citado 29/10/2025];10(2):1-45. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC11888605/pdf/pai-10-001.pdf
- Johnson MM, Odell JA. Nontuberculous mycobacterial pulmonary infections. J Thorac Dis. 2014[citado 20/11/2025];6: 210-20. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC3949190/pdf/jtd-06-03-210.pdf
- Chalmers JD, Aksamit T, Carvalho ACC, Rendon A, Franco I. Non-tuberculous mycobacterial pulmonary infections. Pulmonology Journal. 2018[citado 29/12/2025] ;79(4):e27-e47.
- Lipman M, Kunst H, Loebingere MR, Milburng HJ, King M. Non tuberculous mycobacteria pulmonary disease: patients and clinicians working together to improve the evidence base for care. International Journal of Infectious Diseases. 2021[citado 20/01/2026];5266:5 Disponible en: https://discovery.ucl.ac.uk/id/eprint/10125716/9/Lipman_Non%20tuberculous%20mycobacteria%20pulmonary%20disease%20patients%20and%20clinicians%20working%20together%20to%20improve%20the%20evidence%20base%20for%20care_AOP.pdf
Conflicto de intereses
Los autores declaran que no existió conflicto de intereses.
Contribuciones de autores
Curación de datos: Lázaro Rafael Rodríguez Cabrera.
Análisis formal: Lázaro Rafael Rodríguez Cabrera.
Metodología.: Milena Duque Vizcaino, Ailyn Machado Sosa
Investigación: Lázaro Rafael Rodríguez Cabrera.
Redacción -Borrador original: Lázaro Rafael Rodríguez Cabrera. Ailyn Machado Sosa
Redacción- Revisión Original: Lázaro Rafael Rodríguez Cabrera. Milena Duque Vizcaino
Recursos: Milena Duque Vizcaino. Ailyn Machado Sosa
Supervisión: Lázaro Rafael Rodríguez Cabrera. Milena Duque Vizcaino
Validación: Lázaro Rafael Rodríguez Cabrera. Milena Duque Vizcaino
Revisores: Dr. C. Ventura Puente Saní, Dr. Osvaldo Aguilera Batista
Correctora: MSc. Delaine Núñez Carbonell