MEDISAN 2026;30e5542
Concentrado plaquetario para terapia celular afín al método de obtención
Platelet concentrate for cell therapy according to the obtention method
1Banco de Sangre Renato Guitart Rosell. Santiago de Cuba, Cuba.
Autor para la correspondencia: Karenia.leon@infomed.sld.cu
Recibido: 05/01/2026
Aprobado: 30/01/2026
RESUMEN
Introducción: La terapia celular con el empleo de plaquetas es uno de los pilares que sustentan la medicina regenerativa. Se fundamenta en conductas usadas por el organismo para reemplazar células dañadas por sanas. El uso de las plaquetas con fines regenerativos muestra resultados alentadores, dado el gran número de factores bioactivos y regenerativos contenidos.
Objetivo: Caracterizar el concentrado plaquetario empleado para aplicar en la terapia celular acorde al método de obtención.
Método: Se realizó un estudio descriptivo, transversal, prospectivo en el período comprendido desde 2022 - 2024. La muestra estuvo constituida por 130 concentrados plaquetarios. Las variables fueron: la inspección visual; recuentos celulares y estudios microbiológicos. Se aplicó la estadística descriptiva e inferencial. La correlación entre variables, se realizó mediante pruebas no paramétricas.
Resultados: En la inspección visual 100 % de los concentrados plaquetarios presentaron un color amarillo, ausencia de lipemia, hemólisis, agregados plaquetarios e íctero. Los estudios microbiológicos resultaron negativos. La mayoría de las muestras presentaron heterogeneidad con el fenómeno de turbulencia, los recuentos plaquetarios comprendidos entre 4,1 y 5,5 x 1011/unidad, carecieron de leucocitos y hematíes. Predominó el pH 7.0. Se probó la correlación estadística marcada y positiva entre el recuento plaquetario y fenómeno de turbulencia, ambas variables son dependientes.
Conclusión: La caracterización del concentrado plaquetario obtenido en SAMERSAC para aplicar en la terapia celular regenerativa, permitió obtener un producto homogéneo reproducible de alta confiabilidad, lo que favorece la calidad de los servicios de salud relacionados con su aplicación.
ABSTRACT
Introduction: The cell therapy using platelets is one of the cornerstones of regenerative medicine. It is based on the body's natural processes for replacing damaged cells by healthy ones. The use of platelets for regenerative purposes shows promising results, given the large number of bioactive and regenerative factors contents.
Objective: To characterize the platelet concentrate used in cell therapy according to the obtention method.
Method: A descriptive, cross-sectional, and prospective study was carried out during the period from 2022 to 2024. The sample consisted of 130 platelet concentrates. The variables studied included: the visual inspection; cell counts; and microbiological studies. Descriptive and inferential statistics were applied. The correlation between variables was assessed using non-parametric tests.
Results: In the visual inspection, 100 % of the platelet concentrates showed a yellow color, with no lipemia, hemolysis, platelet aggregates, or jaundice. The microbiological studies were negative. Most samples exhibited heterogeneity with a turbulence phenomenon, with platelet counts ranging from 4.1 to 5.5 x 1011/unit, and were devoid of leukocytes and red blood cells. The pH predominantly measured 7.0. A strong positive statistical correlation was found between platelet count and the turbulence phenomenon, indicating that both variables are dependent.
Conclusion: The characterization of the platelet concentrate obtained at SAMERSAC for use in regenerative cell therapy resulted in a reproducible homogeneous product of high reliability, which enhances the quality of healthcare services related to its use.
Introducción
En los últimos años se ha producido un extraordinario avance en los conocimientos relacionados con la medicina regenerativa. El elemento básico de este tipo de medicina, se sustenta en el proceso que el organismo emplea para remplazar por células sanas a las dañadas mediante diversos mecanismos en determinados tejidos.1 Se encarga de la regeneración y reparación de tejidos y órganos para recuperar su funcionalidad.2
El inicio del siglo XXI marca el desarrollo de la TCR en el mundo, aplicada en países de Asia, Europa y en algunos de Latinoamérica como Brasil, México, Uruguay y Argentina.3 En Cuba se introduce en el 2004 por el Dr. C. Porfirio Hernández Ramírez, promotor del uso de plaquetas, tanto autólogas como alogénicas, con fines regenerativos.3
A partir del 2008 el empleo de las plaquetas con fines regenerativos se incrementó de forma progresiva, extendiéndose a todo el país, debido a que su obtención no requiere procesamiento especial, mediante técnica de centrifugación se separan las plaquetas de la sangre periférica.4
En el 2011 se introduce en la provincia y se crea el Servicio Ambulatorio de Medicina Regenerativa de Santiago de Cuba (SAMERSAC), como nuevo servicio científico tecnológico, dedicado a la obtención de hemocomponentes con fines regenerativos.5
En el presente estudio, los parámetros de calidad de los concentrados plaquetarios (CP) se analizaron a partir de las referencias de los estándares de la Asociación Americana para Bancos de Sangre (AABB),6 la Fundación para la Acreditación de Terapia Celular7 y las normativas nacionales establecidas por el órgano regulatorio cubano (CECMED).8
Cabe destacar, que el número de publicaciones relacionadas con el uso de las plaquetas con fines regenerativos, se incrementa y muestran resultados alentadores, debido al gran número de factores bioactivos y regenerativos contenidos en ellas. Múltiples estudios señalan que el tratamiento con plaquetas produce mejorías clínicas significativas y resultados funcionales con menos efectos adversos.9
A pesar del amplio uso de las plaquetas en varios países, se considera que existen muchas divergencias e inconsistencias en los métodos de preparación entre los diferentes grupos de investigación, por lo que se recomienda, la caracterización de este componente sanguíneo para garantizar resultados comparables y reproducibles.
Cao y colaboradores10 plantean, que la variación en los métodos para producir concentrados plaquetarios tienen relación directa con las diferencias en los tiempos de centrifugación, distintas fuerzas centrífugas, diferencia de longitud del eje, el diámetro, longitud del tubo de la centrífuga y el material del tubo, todo lo cual influye en el producto final obtenido.
Con relación a la investigación, se caracterizaron los CP que se utilizaron en el servicio para preparar el lisado plaquetario; por lo que se tuvo en cuenta diferentes variables lo que permitió evaluar la calidad y seguridad del producto biológico obtenido y así garantizar su aplicación en la terapia celular regenerativa.
En el estudio se tuvo en cuenta las características propias del servicio, el equipamiento empleado en el procesamiento, obtención y estudios analíticos de los CP, con la finalidad de elegir los valores que informen sobre la calidad y seguridad del producto biológico utilizado en la implantación a los pacientes, de manera que asegure la efectividad del tratamiento. Por tal motivo se trazó como objetivo caracterizar el concentrado plaquetario empleado para aplicar en la terapia celular acorde al método de obtención.
Método
Se realizó una investigación descriptiva y prospectiva, en el período comprendido desde septiembre del 2022 hasta mayo del 2024, en el Servicio Ambulatorio de Medicina Regenerativa del Banco de Sangre Provincial de Santiago de Cuba, con el propósito de caracterizar el CP empleado para aplicar la terapia celular acorde al método de obtención.
Cabe destacar que se utilizaron variables de interés de acuerdo a la tecnología de procesamiento, evaluación de parámetros de calidad y seguridad de los componentes sanguíneos, las que permitieron caracterizar este producto celular empleado para la TCR como una nueva alternativa terapéutica.
Se realizaron pruebas de inspección visual, (aspecto, color, presencia de agregados), pH, fenómeno de turbulencia o remolino y recuentos celulares mediante la cámara de Neubauer y microscopio óptico. Se realizaron además estudios microbiológicos (bacteriológicos, serológicos y virológicos).
La población estuvo conformada por 193 CP. Se escogió una muestra de 130 por medio de una calculadora automática para el cálculo del tamaño de la muestra, con un intervalo de confianza del 95,0 %, y un nivel de significación del 5,0 %, error α de 5,0 %.
Resulta oportuno aclarar que los datos fueron recogidos de los resultados emitidos por el laboratorio de la entidad. Se creó una base de datos en Excel, procesada en el programa estadístico SPSS versión 22. Se aplicó la estadística descriptiva e inferencial. A las variables cualitativas se les analizó medidas de frecuencia como porcentaje, para saber cómo estaban distribuidos los datos; para las variables cuantitativas se calcularon medidas de tendencia central, media y desviación estándar.
Resultados
Se analizaron 130 CP obtenidos a partir de sangre total periférica, que fueron caracterizados de acuerdo con las variables establecidas en la investigación. El 100 % de los estudios bacteriológicos (crecimiento de microorganismos), serológicos (VRDL) y virológicos (VIH 1/2, HBsAg, VHC) fueron negativos.
En cuanto a la inspección visual, 100 % de los CP presentaron color amarillo, con ausencia de lipemia, hemólisis e íctero. No hubo presencia de agregados plaquetarios, ni contaminación hemática visible.
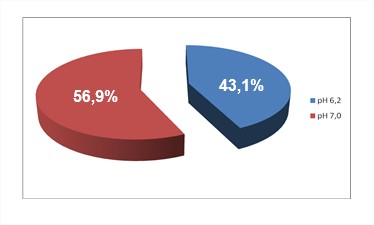
Al evaluar la determinación del pH, no se muestran valores fuera del rango establecido para los componentes sanguíneos, con intervalos de pH entre 6,2 y 7,0. Predominó el pH 7.0 en 56,9 % (Figura 1).
Fig 1: Determinación pH del CP
El promedio de recuento plaquetario fue de 4,3 x1011 plaquetas/unidad, con una DE de 2,5. El 26,2 % de las unidades evaluadas tienen un recuento plaquetario mayor de 5,5 x 1011/unidad, seguido del grupo comprendido entre 4,1 a 5,5 x 1011/unidad (20,8 %) y los rangos 2,1 a 3,0 x 1011/unidad con un 20,0 %, como se muestra en la tabla 1.
Tabla 1: Conteo de plaquetas en los concentrados plaquetarios

En el recuento leucocitario que se muestra en la tabla 2 el valor promedio fue de 0,07 x109/unidad con una DE 0,2. El 46,2 % de las unidades evaluadas carecieron de leucocitos (60), seguidos del rango entre 0,01-0,09 x109/L (51) para un 39,2 %. Solo 1,5 % presentó más de 1,0 x109/L leucocitos.
Tabla 2: Conteo de leucocitos en los concentrados plaquetarios

El promedio de eritrocitos residuales fue de 0,07 x106/unidad (tabla 3). En 61,5 % de los CP analizados no se probó la presencia de hematíes en el conteo, seguidos de los que se encontraron en el rango (0,01 - 0,09) x 106/unidad, representados por un 34,6 %.
Tabla 3: Conteo de eritrocitos en los concentrados plaquetarios

El 71,5 % de las unidades evaluadas (93) desarrollaron el fenómeno de turbulencia de forma heterogénea mientras que 28,5 % fue poco heterogéneo (tabla 4). En los concentrados que mostraron recuentos plaquetarios ≥3,1 x1011plaquetas/unidad el fenómeno de turbulencia apareció de forma heterogénea.
Al realizar las pruebas estadísticas de Pearson y Spearman, se probó una correlación estadística marcada y positiva con p< 0,05. Al aplicar la prueba no paramétrica de U Mann Whitney, se pudo afirmar que con un 95,0 % de confianza, ambas variables son dependientes una de la otra.
Tabla 4: Fenómeno de turbulencia según el conteo de plaquetas

Discusión
La terapia con plaquetas ha acumulado una atención considerable durante las dos últimas décadas, principalmente en el área de la TCR, por su capacidad regeneradora y reparadora de tejidos y órganos para recuperar su funcionalidad. Es empleada como alternativa de tratamiento en diferentes enfermedades, que muchas veces carecen de un tratamiento efectivo.
Se visualizan en la comunidad científica innumerables artículos que muestran valiosos resultados desde el punto de vista clínico, pero existe diversidad de criterios relacionados con el contenido de este producto biológico. Por esta razón y sobre el conocimiento de los estándares nacionales e internacionales, se justifica la presente investigación.
La misma tiene su base en la creación de un servicio científico tecnológico que demanda de un sistema de calidad, que implica introducir el empleo de los medios diagnósticos para establecer sus propios estándares, acorde con sus condiciones.
El implemento de la evaluación de las tecnologías especializadas en los sistemas de salud, no solo ha sido motivada por la necesidad de contar con un proceso legítimo basado en la prueba científica, sino también, en la necesidad de mejorar la eficiencia y calidad de los servicios.11
La presente investigación centró su estudio en la estandarización de parámetros de calidad de las plaquetas, sobre la base del conocimiento del gran potencial regenerativo en los tejidos, ya que favorece la angiogénesis, migración, diferenciación y proliferación celular debido a su alto contenido en factores de crecimiento.12
La inspección visual fue el primer parámetro de calidad evaluado en los concentrados plaquetarios utilizados con fines regenerativos. Se aseguró su calidad para la elaboración del lisado plaquetario (LP). Resultados similares obtuvo González Iglesia3 en el 2014, quién plantea que 100 % de los CP cumplieron con el aspecto físico, color, ausencia de agregados y producción en sistema cerrado.
El pH es un parámetro de calidad que nos indica los niveles de alcalinidad y acidez del medio en el que se encuentran las plaquetas; en el caso de alcalinización del medio se podría sospechar la presencia de agentes bacterianos. En el presente estudio 100 % de las unidades tenía pH acorde con los parámetros dispuestos por la AABB.6 Este resultado probó que el mayor número de CP mantuvo un pH neutro, en el cual se conservan las plaquetas, lo que garantiza la calidad del producto obtenido (figura 1).
El pH es un parámetro importante porque determina la viabilidad de las plaquetas. Los valores por debajo de 6,0 indican que las plaquetas se vuelven esféricas, cuyo cambio es irreversible, su metabolismo se detiene y pierden su funcionalidad y actividad regenerativa.
Huayta Osco MA13 en su reciente estudio plantea que el nivel normal de pH en el CP es de 6.2 a 7.4 y que la disminución podría afectar la funcionabilidad una vez administradas, lo que coincide con la casuística analizada en este trabajo. El pH también indicaría cambios metabólicos de leucocitos residuales al incrementar el ácido láctico, lo que genera una mala calidad del CP.
La determinación del pH es un método que permite evaluar la calidad de las plaquetas. Los valores de pH bajos en estos concentrados provocan lesiones irreversibles y afectan su función regenerativa. Bermejo González M14 en su estudio encontró que los resultados de pH obtenidos para los lisados plaquetarios investigados, tuvieron en el rango de 7,0 a 8,0 con variabilidad del pH neutro.
El recuento de plaquetas fue el principal parámetro para la caracterización de los concentrados, por ser estas células consideradas como responsables de los efectos terapéuticos en diversas enfermedades. Son protagónicas en el proceso de reparación tisular; liberan mediadores bioquímicos como las citoquinas y quimioquinas, constituyen un reservorio de un alto contenido en factores de crecimiento y otras sustancias con capacidad regenerativa.
En el recuento de plaquetas el mayor porciento obtuvo un conteo ≥4,1x1011/unidad (tabla 1). Pérez C15 en su trabajo desarrolló un método de obtención de CP, el cual permitió alcanzar una adecuada concentración en los preparados, similar a los alcanzados en la presente investigación; sin embargo, Bianchetti A16 difiere al plantear que en su casuística predominaron recuentos más bajos (1 x 106 plaquetas por unidad). Bermejo González M14 en diferentes grupos estudiados encontró que la concentración de plaquetas estaba por debajo de los resultados de la presente investigación.
El rendimiento plaquetario en esta investigación es satisfactorio y óptimo para asegurar una cantidad de factores de crecimiento necesarios para la reparación de tejidos dañados y mejorar la calidad de vida del enfermo al aplicar esta nueva alternativa terapéutica.
El recuento de leucocitos residuales en el CP indica un parámetro de calidad importante para el implante de este producto biológico. Los leucocitos compiten con las plaquetas por los nutrientes, lo que afecta la calidad del concentrado que se desea utilizar en un enfermo para la regeneración celular.
Lo antes expuesto explica la necesidad de obtener un producto con una concentración mínima de leucocitos, para darle una mayor calidad, lo que se logró en el presente estudio con la adecuada estandarización del proceso tecnológico en SAMERSAC, para asegurar el servicio brindado a los enfermos seleccionados para el implante del LP.
En el recuento leucocitario residual, la mayoría de las unidades investigadas tuvo ausencia de estas células, seguidas de las que mantuvieron un conteo < 0,1x109/unidad (tabla 2), lo que indica muy poca contaminación con este tipo de célula y se cumple con el valor de referencia indicado en el Manual Técnico Asociación Americana para Bancos de Sangre.6 Arroyo Rubio CE17 demostró que 100 % de sus CP contó con un recuento óptimo de leucocitos residuales (<0.12×109/unidad), resultado que coincide con el presente trabajo. En el año 2021, Cienfuegos Pecina E18 obtuvo como resultado, que 50,0 % de los concentrados plaquetarios cumplió con todos los requisitos del control de calidad.
La actividad metabólica de los leucocitos contamina el producto, ya que tienen la tendencia de producir mayor cantidad de ácido láctico. Si existiera un alto número de leucocitos en el concentrado, las plaquetas producirían más ácido láctico, lo cual provocaría una baja del pH. El metabolismo de las plaquetas cesa por completo cuando los valores del pH son menores a 6,0.19
El recuento de eritrocitos residuales analizado en esta investigación se encuentra dentro de los límites establecidos por la Asociación Americana para Bancos de Sangre,6 acorde con las preparaciones de plaquetas de acuerdo al método de obtención. La mayoría de los preparados evaluados no se encuentran contaminados con esta célula (tabla 3).
González Iglesia3 en su investigación, realiza una caracterización de los concentrados plaquetarios utilizados en la terapia celular y obtiene conteos de eritrocitos entre 0,01 y 0,03 × 1012 /L; resultados muy cercanos a los obtenidos en el presente trabajo.
Arroyo Rubio CE17 en el recuento de células realizado a los CP encontró que 7,3 % sobrepasó el límite de eritrocitos residuales (<1.2×106 células/unidad), resultado que difiere del presente estudio, donde el mayor porcentaje de las muestras estudiadas está entre 0-0,09×106/unidad.
La medición del fenómeno de turbulencia o remolino, constituye el parámetro que mejor predice la cantidad de plaquetas responsables de la regeneración de tejidos dañados en distintas partes del organismo.
La presencia del remolino evaluado a contra luz permitió categorizar esta variable según su heterogeneidad. La mayoría de las unidades evaluadas muestran un aspecto heterogéneo. Esta prueba es una forma de evaluar que aún se mantiene la forma discoidal de las plaquetas, lo que indica la viabilidad de esta célula. La ausencia de remolino es un indicador de que estas se han vuelto esféricas. El fenómeno de turbulencia o remolino resulta ser un método sencillo para evaluar las características morfológicas de las plaquetas (tabla 4).
La formación del torbellino plaquetario evaluado por Arroyo Rubio CE17 en su casuística, demostró que 58.3 % de los CP presentaron una formación de 3 cruces de heterogeneidad el primer día de procesado; resultado semejante se alcanza en este estudio.
Al relacionar fenómeno de turbulencia con el conteo plaquetario, se demuestra una relación directa entre ambos parámetros, es decir a mayor concentración de plaquetas más heterogéneo resulta el fenómeno de turbulencia (tabla 4) y mayor calidad se alcanza en el producto biológico obtenido.
En la bibliografía se plantea que el objetivo de cualquier método no es solo la seguridad y la eficacia, sino la obtención de un producto final con características muy definidas, un preparado estéril, con una concentración optima de plaquetas y factores de crecimiento, y un contenido celular ajustado a las necesidades terapéuticas y al criterio del especialista.20
La caracterización del concentrado plaquetario obtenido en SAMERSAC para aplicar en la terapia celular regenerativa, permitió obtener un producto homogéneo reproducible de alta confiabilidad, lo que favorece la calidad de los servicios de salud relacionados con su aplicación.
Referencias Bibliográficas
- Turiño Peña H, Duperet Carvajal D, Audivert Hung Y, Pérez Pérez M. Plasma rico en plaquetas, una alternativa de tratamiento en la úlcera corneal recurrente Acta Médica. 2022[citado 22/5/2023]; 23(4):e272. Disponible en: https://revactamedica.sld.cu/index.php/act/article/view/272/pdf
- Blanco Amaro EC, Gámez Pérez A, Falcon Díaz JL. Lisado plaquetario en el tratamiento de la fisura anal crónica y otras indicaciones. Revista Cubana de Medicina. 2022[citado 23/4/2024]; 61(4):e2923. Disponible en: https://revmedicina.sld.cu/index.php/med/article/view/2923/2365
- González Iglesias AI, Fernández Delgado N, Forrellat Barrios M, Hernández Ramírez P. Caracterización de los concentrados plaquetarios utilizados en Medicina Regenerativa. Rev Cubana Hematol Inmunol Hemoter. 2014[citado 22/5/2023]; 30(2): 171-78. Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S0864-02892014000200010&lng=es
- Tornero Tornero JC, Fernández Rodríguez LE. Plasma rico en plaquetas y células madre mesenquimales intrarticulares en artrosis. RESED. 2021[citado 21/2/2022]; 28(1): 80-4. Disponible en: https://scielo.isciii.es/pdf/dolor/v28s1/1134-8046-dolor-28-s1-0080.pdf
- Ali Pérez NA, Robinson Rodríguez RJ, Hernández Ramírez P. Nueva tecnología sanitaria para el desarrollo de la medicina regenerativa en Santiago de Cuba. Rev Cubana Hematol Inmunol Hemoter. 2019[citado 10/10/2022]; 35(3):e934. Disponible en: http://scielo.sld.cu/pdf/hih/v35n3/1561-2996-hih-35-03-e934.pdf
- Association for the Advancement of Blood & Biotherapies. Technical Manual: Methods and appendices.20th ed. [s.l]: AABB; 2020[citado 22/5/2023]. Disponible en: https://www.aabb.org/aabbstore/product/technical-manual-20thedition---digital-14885335
- FACT J. Estándares internacionales para la recolección, procesamiento y administración de productos hematopoyeticos de terapia celular. 8ª ed Nebraska FACT; 2021[Consultado 12/3/2023]. Disponible en: https://www.ebmt.org/sites/default/files/2021-08/Estándares Internacionales FACT-JACIE Octava Edicion Completa.pdf
- Cuba. Ministerio de Salud Pública. Centro para el Control Estatal de los Medicamentos Equipos y Dispositivos Médicos (CECMED). Resolución CECMED No. 63/2020: Regulación M 91-20. Especificaciones de calidad de la sangre obtenida por donación y de sus componentes. La Habana: CECMED; 2020 [citado 22/5/2023]. Disponible en: https://www.cecmed.cu/sites/default/files/adjuntos/Reglamentacion/Res.RegWEB.pdf
- Belk JW, Kraeutler MJ, Houck DA, Goodrich JA, Dragoo JL, McCarty EC. Platelet-Rich Plasma Versus Hyaluronic Acid for Knee Osteoarthritis: A Systematic Review and Meta-analysis of Randomized Controlled Trials. The American journal of sports medicine. 2021[Consultado 12/3/2023]; 49(1): 249-60. Disponible en: https://journals.sagepub.com/doi/full/10.1177/0363546520909397
- Cao Y, Zhu X, Zhou R, He Y, Wu Z, Chen Y. A narrative review of the research progress and clinical application of platelet-rich plasma. APM. 2021[Consultado 12/3/2023]; 10(4): 4823-29. Disponible en: https://apm.amegroups.org/article/view/63809/html
- Pérez Andrés IY, Salas Palacios SR, Robinson Rodríguez RJ, Travieso Ramos N. Implementación de una metodología formativa para la gestión en el proceso de evaluación de tecnologías sanitarias. MEDISAN. 2021[Consultado 3/6/2024]; 25(4): 1047-59. Disponible en: http://scielo.sld.cu/scielo.php?pid=S1029-30192021000401047&script=sci_arttext&tlng=pt
- López Quinga NS. El plasma rico en plaquetas como una estrategia prometedora para el tratamiento del síndrome de Asherman. Revista Científica Arbitrada Multidisciplinaria PENTACIENCIAS. 2023[Consultado 3/6/2024]; 5(6): 384-99. Disponible en: https://editorialalema.org/index.php/pentaciencias/article/view/863/1179
- Huayta Osco MA. Parámetros de calidad de concentrados de plaquetas, en medición basal, quinto y séptimo día, en el banco de sangre del hospital III Daniel Alcides Carrión. TESIS. Perú: UNIVERSIDAD PRIVADA DE TACNA; 2022[Consultado 12/3/2023]. Disponible en: https://repositorio.upt.edu.pe/bitstream/handle/20.500.12969/2470/Huayta-Osco-Maria.pdf?sequence=1
- Bermejo González M. Caracterización de productos empleados en la fabricación de medicamentos de terapias avanzadas. Tesis Doctoral. España: Universidad de Sevilla; 2022[Consultado 12/3/2023] Disponible en: https://idus.us.es/server/api/core/bitstreams/3d3cf69e-45fd-4b50-996b-001fb4fafe5a/content
- Pérez C, Escobar G, Soto P, Ibarra C, Larrondo M, Alfar J. Obtención de plasma rico en plaquetas en el Laboratorio de Terapia Celular para uso como herramienta terapéutica en medicina regenerativa. Rev Hosp Clín Univ Chile. 2021[Consultado 12/3/2023]; 32: 4-16. Disponible en: https://www.redclinica.cl/Portals/0/Users/014/14/14/1950.pdf
- Bianchetti A, Chinello C, Guindani M, Braga S, Neva A, Verardi R, et al. A Blood Bank Standardized Production of Human Platelet Lysate for Mesenchymal Stromal Cell Expansion: Proteomic Characterization and Biological Effects. Front Cell Dev Biol. 2021[Consultado 12/3/2023]; 9. Disponible en: https://www.frontiersin.org/journals/cell-and-developmental-biology/articles/10.3389/fcell.2021.650490/full
- Arroyo Rubio CE, Jaramillo Ruales KE, Chiriboga Ponce RF. Determinación de la viabilidad de los concentrados plaquetarios obtenidos de capa leucocitaria durante siete días de almacenamiento. Rev. Cienc. Salud. 2021[Consultado 12/3/2023]; 19(3): 1-13. Disponible en: http://www.scielo.org.co/pdf/recis/v19n3/2145-4507-recis-19-03-121.pdf
- Cienfuegos Pecina E, Leal Nava ER, Avilés Rodríguez LE, Llaca Díaz JM, Pérez Chávez F, Cázares Tamez R, et al. Donor platelet and leukocyte count as predictive factors of the quality of platelet concentrates obtained from whole blood by semiautomated fractionation. Transfus Apher Sci. 2021[Consultado 12/3/2023]; 60(1): e102972. Disponible en: https://www.sciencedirect.com/science/article/abs/pii/S1473050220302883
- Contreras Aliano MG, Huayta Franco YJ, Chumpitaz Panta J, Caro Zamora JR. Evaluación de la eficacia en la colecta de plaquetas por un separador celular. Revista de Investigación en Salud. 2022[Consultado 12/3/2023]; 5(15): 947-59. Disponible en: https://portal.amelica.org/ameli/journal/541/5413580023/5413580023.pdf
- Morales Portillo CA, Delgado San Vicente D, García Henares JF, Ruiz Ramírez JC, Muñoz Ortego J, Torres Morera LM. Uso de plasma rico en plaquetas (PRP) y derivados en el tratamiento del dolor: guía de consenso de la SEMDOR 2025. Revista de la sociedad española multidisciplinar del dolor. 2025[Consultado 12/3/2023]; 5: 130-42. Disponible en: https://www.mpainjournal.com/uso-de-plasma-rico-en-plaquetas-prp-y-derivados-en-el-tratamiento-del-dolor-guia-de-consenso-de-la-semdor-20257240
Conflicto de intereses
Los autores declaran que no hubo conflicto de intereses alguno.
Contribución de los autores
Lic. Karenia León Munive, Niurka Aurora Ali Pérez: conceptualización de las ideas, desarrollo y diseño metodológico de la investigación; redacción del manuscrito, aprobación del trabajo final (70 %).
Lic. Dunia Rodríguez Vargas: análisis y procesamiento de los datos (20 %).
Lic. Mercedes Vega Pérez, Lic. Iradelmis Vaillant Beltrán: revisión bibliográfica (10 %).
Revisores: Dr. C. Níger Guzmán Pérez, MSc. Rafael Escalona Veloz.
Corrector: Lic. Alexander Brossard Taureaux.