MEDISAN 2026;30:e5543
Estratificación del riesgo de crisis vaso-oclusivas en la anemia falciforme mediante biomarcadores redox
Risk stratification of vaso-occlusive crises in sickle cell anemia using redox biomarkers
1Centro de Biofísica Médica. Santiago de Cuba, Cuba.
2Universidad de Ciencias Médicas. Santiago de Cuba, Cuba.
3Hospital Juan Bruno Zayas Alfonzo. Santiago de Cuba, Cuba.
4Juan Bruno Zayas Alfonzo. Santiago de Cuba, Cuba.
5Centro de Biofísica Médica. Santiago de Cuba, Cuba.
Autor para la correspondencia: Correo electrónico: yalonso09@gmail.com
Recibido: 26/01/2026
Aprobado: 07/03/2026
RESUMEN
Introducción: Las manifestaciones clínicas de la anemia falciforme son muy heterogéneas, lo que dificulta la predicción de eventos agudos. Resulta necesario establecer asociaciones entre marcadores bioquímicos y el riesgo de complicaciones agudas. El estado redox desempeña una función crucial en la fisiopatología de la enfermedad y puede ser un biomarcador predictivo de la crisis vaso-oclusivas.
Objetivo: Aplicar una escala de riesgo basada en biomarcadores del estado redox (glutatión reducido y malondialdehído) en la estratificación del riesgo de crisis vaso-oclusivas en una cohorte de pacientes con anemia falciforme en Santiago de Cuba.
Métodos: Se realizó un estudio analítico longitudinal en 72 pacientes con anemia falciforme de Santiago de Cuba en el periodo julio-diciembre de 2022. Se aplicó una escala de riesgo derivada del análisis discriminante lineal a partir de las concentraciones de malondialdehído y glutation reducido. La capacidad discriminatoria de la escala se evaluó mediante el área bajo la curva ROC.
Resultados: La escala mostró una asociación marcada y significativa con el estado clínico (p<0,001). La escala simplificada demostró una excelente capacidad discriminatoria (AUC de 0,957). La sensibilidad y el valor predictivo negativo fueron del 100 %, lo que identifica correctamente a todos los pacientes que desarrollaron complicaciones. La especificidad fue del 90,9 %.
Conclusiones: La escala de riesgo aplicada demuestra un desempeño marcado y alto valor predictivo negativo en esta cohorte. Su implementación permite la estratificación de riesgo de crisis vaso-oclusivas en la anemia falciforme.
ABSTRACT
Introduction: The clinical manifestations of sickle cell anemia are highly heterogeneous, making it difficult to predict acute events. Establishing associations between biochemical markers and the risk of acute complications is essential. Redox status plays a crucial role in the pathophysiology of the disease and may be a predictive biomarker for vaso-occlusive crises.
Objective: To Apply a risk scale based on redox status biomarkers (reduced glutathione and malondialdehyde) in the risk stratification of vaso-occlusive crises in a cohort of patients with sickle cell anemia in Santiago de Cuba.
Methods: A longitudinal analytical study was carried out in 72 patients with sickle cell anemia in Santiago de Cuba between July and December 2022. A risk scale derived from linear discriminant analysis was applied using malondialdehyde and reduced glutathione concentrations. The discriminatory capacity of the scale was evaluated using the area under the ROC curve.
Results: The scale showed a strong and significant association with clinical status (p<0.001). The simplified scale demonstrated excellent discriminatory ability (AUC of 0.957). Sensitivity and negative predictive value were both 100 %, correctly identifying all patients who developed complications. Specificity was 90.9 %.
Conclusions: The applied risk scale demonstrates robust performance and high negative predictive value in this cohort. Its implementation allows for the risk stratification of vaso-occlusive crises in sickle cell anemia.
INTRODUCCIÓN
La anemia falciforme (AF) constituye una de las hemoglobinopatías hereditarias más frecuentes a nivel mundial. Es producida por una mutación puntual del gen de la cadena β-globina de la hemoglobina, dando lugar a una hemoglobina anormal denominada hemoglobina S (HbS) que tiende a polimerizar en condiciones de desoxigenación.1 Los mecanismos fisiopatológicos clásicos de la AF son la polimerización de la HbS, falciformación de los eritrocitos SS y la vaso-oclusión; sin embargo, más recientemente se ha descrito la importancia de otros mecanismos en su fisiopatología, como el incremento de hemoglobina libre, aumento del estrés oxidativo, disminución local de óxido nítrico y liberación de mediadores inflamatorios.2 Todos estos mecanismos producen una importante disfunción endotelial que conduce complicaciones agudas y crónicas.3,4
La expresión clínica de la AF presenta una amplia heterogeneidad, lo que dificulta la predicción de eventos agudos. Si bien se han identificado asociaciones entre factores sociodemográficos y ambientales con la ocurrencia de las crisis vaso-oclusivas (CVO), dichas asociaciones son fundamentalmente fenomenológica, por lo que resulta necesario establecer asociaciones entre marcadores bioquímicos, particularmente aquellos vinculados a la fisiopatología central de la enfermedad, y el riesgo de complicaciones agudas.5
La estratificación precisa del riesgo de CVO sigue siendo un desafío en la práctica clínica, lo que ha impulsado la búsqueda de biomarcadores predictivos confiables. En este contexto, el estado redox desempeña un función crucial en la fisiopatología de la AF, ya que se incrementa la generación de especies reactivas de oxígeno (ERO) y se alteran los sistemas antioxidantes endógenos. Biomarcadores como el glutatión reducido (GSH), principal antioxidante intracelular; el malondialdehído (MDA), producto final de la peroxidación lipídica y la actividad de enzimas antioxidantes podrían ofrecer información relevante del estrés oxidativo en la AF y ser indicadores útiles para predecir las CVO.6
Dado lo anteriormente expuesto, las escalas que integren estos biomarcadores ofrecen una vía para la estratificación de riesgo. En este estudio se aplica la escala propuesta por Cruz H 7 basada en biomarcadores del estado redox (GSH y MDA), la cual ha demostrado un alto poder discriminativo en estudios, en una nueva cohorte de pacientes con AF para validar su utilidad práctica en la estratificación del riesgo de CVO.
MÉTODOS
Se realizó un estudio observacional, analítico, longitudinal y ambispectivo en una cohorte de 72 pacientes con AF, seleccionados consecutivamente durante sus consultas de seguimiento, en el Hospital "Juan Bruno Zayas" de Santiago de Cuba, en el periodo julio-diciembre de 2022. Se obtuvo el consentimiento informado de los pacientes previo a su inclusión en el estudio.
Criterios de inclusión:
- Pacientes con diagnóstico molecular de hemoglobinopatía SS (HbSS) mediante electroforesis de Hb4
- Edad mayor o igual a 19 años
- Estado clínico basal al momento del reclutamiento
Criterios de exclusión:
- Diagnóstico de otras hemoglobinopatías
- Presencia de comorbilidades (insuficiencia hepática severa o insuficiencia renal crónica avanzada) que pudiesen actuar como variables confusoras.
Definiciones Clínicas
Los estados clínicos (estado basal, CVO y comorbilidades) fueron establecidos por los especialistas en hematología de acuerdo al Manual de normas del tratamiento del paciente drepanocítico.7
Aplicación de la Escala de Riesgo
Se aplicó la escala de riesgo de complicaciones agudas en la AF desarrollada por Cruz H7 que se sustenta en un Índice de Riesgo (IR) calculado mediante la ecuación:
IR = 0,439 * C(MDA) - 0,640 * C(GSH) - 1,378 (1)
Donde: C(MDA) y C(GSH): concentraciones de MDA (μmol/L) y GSH (nmol/100mL), respectivamente.
Estratificación del riesgo:
- Escala 1 (original: 3 categorías):
- Riesgo menor: IR < 0,019
- Riesgo moderado: 0,019 ≤ IR ≤ 1,456
- Riesgo mayor: IR > 1,456
- Escala 2 (simplificada: 2 categorías):
- Riesgo menor/moderado: IR ≤ 1,244
- Riesgo mayor: IR > 1,244
Determinaciones de Biomarcadores
Las concentraciones de MDA y GSH se cuantificaron en plasma siguiendo los métodos estandarizados previamente por Cruz H.8
- Determinación de la concentración de MDA mediante la reacción del cromógeno N-metil-2-fenilindol con MDA a 586 nm.9 Se empleó una curva de calibración con de 1,1,3,3-tetrametoxipropano (0-13,20 μmol/L).
- Determinación de la concentración de GSH mediante la reacción colorimétrica con ácido 5,5'ditio-bis 2-nitrobenzóico a 412 nm.10 Se empleó una curva patrón de GSH (1,17-10,54 nmol/100mL).
Análisis estadístico
El análisis estadístico se realizó mediante el software SPSS v25.0 (GNU General Public License, Free Software Foundation). Las variables categóricas se presentan como frecuencias (porcentajes) y las continuas con distribución normal como media ± desviación estándar (DE). La normalidad se verificó con la prueba de Kolmogorov-Smirnov. Para la comparación de medias se utilizaron las pruebas Chi cuadrado para variables categóricas y t de Student para variables continuas. La capacidad discriminatoria se cuantificó mediante el área bajo la curva ROC (AUC-ROC), con intervalos de confianza del 95,0 % (IC 95,0 %).11 Se calculó: sensibilidad, especificidad, valor predictivo positivo (VPP), valor predictivo negativo (VPN) y el índice F1. El punto de corte óptimo se identificó mediante el índice de Youden (J). Para todas las pruebas se estableció un nivel de significación estadística de 0,05.
Consideraciones éticas
La investigación y el uso de datos de los pacientes se realizaron de acuerdo con los principios éticos del Protocolo de Helsinki sobre las investigaciones médicas en humanos y las buenas prácticas de laboratorio;12 se garantizó la privacidad y confidencialidad de los pacientes. Se obtuvo el consentimiento informado de los pacientes de participar voluntariamente en el estudio, previa autorización del Comité de ética y el Consejo Científico del hospital.
RESULTADOS
Caracterización de la muestra de evaluación
De los 550 pacientes con AF registrados en el Hospital Juan Bruno Zayas de Santiago de Cuba, 363 (66,0 %) presentaban el genotipo HbSS. De estos, se excluyó el 76,6 % por falta de datos de seguimiento, y el 4,1 % por datos clínicos y de laboratorio incompletos. La cohorte final incluyó 72 pacientes HbSS, lo que representa el 19,8 % de los pacientes con este genotipo.
Se comparó la cohorte de evaluación (n=72) con la cohorte de estimación del modelo desarrollado por Cruz H.7 Los resultados se presentan en la Tabla 1 como frecuencias (porcentajes) para variables categóricas y media ± DE para continuas.
Tabla 1. Estadígrafos descriptivos y comparación entre cohortes (estimación vs evaluación) para un nivel de significación de α=0,05.
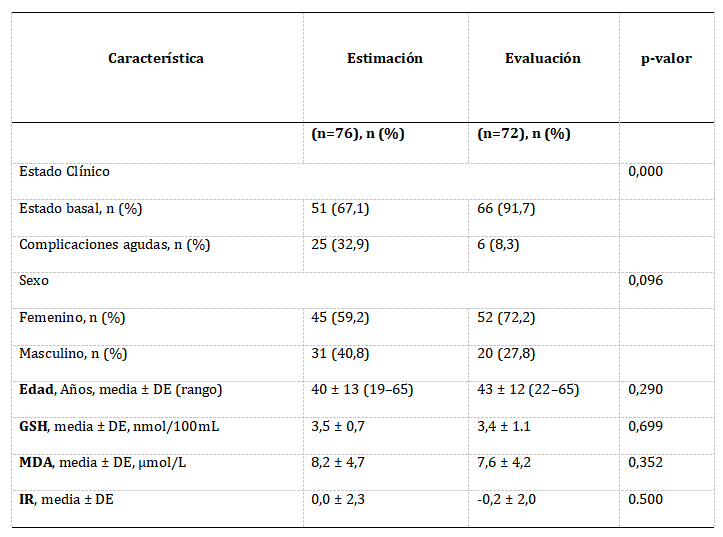
Abreviaturas: GSH: glutatión reducido; MDA: malondialdehído; IR: índice de riesgo; DE: desviación estándar.
Aplicación de la escala de riesgo
Al aplicar la escala de riesgo en la cohorte de estudio se obtuvo una distribución heterogénea entre las tres categorías establecidas: 40 casos (55,6 %) riesgo menor, 20 (27,8 %) riesgo moderado y 12 (16,7 %) riesgo mayor.
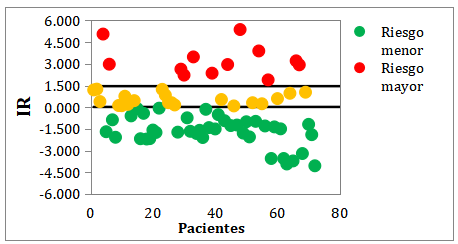
Fig. 1. Representación gráfica de la distribución de los IR para cada categoría.
Optimización de la escala de riesgo
La escala original fue reevaluada considerando que el grupo de riesgo moderado no mostró utilidad clínica como categoría distintiva, ya que el 100 % de los pacientes clasificados en él (20/20) se encontraban en estado basal. Se simplificó la escala a una versión dicotómica (riesgo menor/moderado vs. riesgo mayor).
Como puede observarse en la Figura 2, al agrupar riesgo menor y moderado (punto de corte de 1.456), se mantiene que el 9,1 % es clasificado de Riesgo mayor.
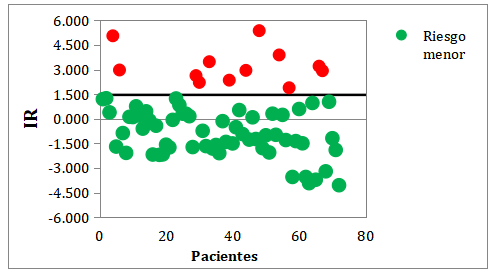
Fig. 2. Distribución del índice de riesgo (IR) de crisis vaso-oclusiva en la anemia falciforme de acuerdo a la escala simplificada. La línea sólida representa el punto de corte establecido (1,456).
La escala de riesgo demostró una capacidad discriminativa excelente con un AUC de 0,957 (IC 95 %: 0,911-1,000; p<0,001) como se aprecia en la curva ROC de la Figura 3.
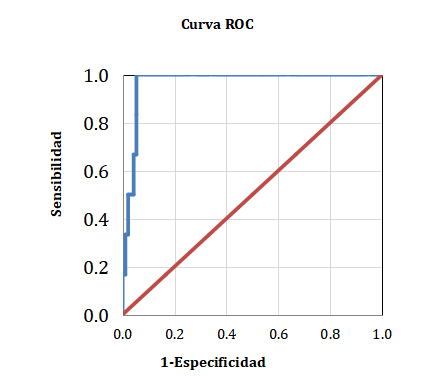
Fig. 3. Curva ROC de la clasificación del riesgo de crisis vaso-oclusiva en la anemia falciforme.
A partir de esta curva se determinó el punto de corte óptimo en 2,055 según el criterio de maximización del índice de Youden (J=0,924) que representa el mejor equilibrio entre sensibilidad y especificidad para esta población. En la Tabla 2 se muestran los resultados del desempeño de la escala para el punto de corte original (U=1,456) y el punto de corte óptimo (U=2,055).
Tabla 2. Rendimiento diagnóstico de la escala de riesgo simplificada de crisis vaso-oclusiva según los puntos de corte U=1,456 y U=2,055.
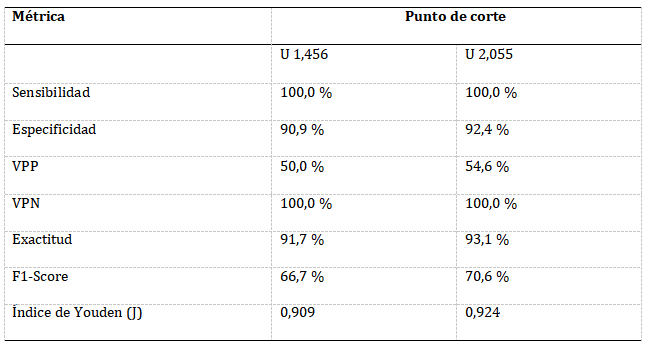
Abreviaturas: U: punto de corte, VPN: valor predictivo negativo, VPP: valor predictivo positivo.
Evaluación de los casos falsos positivos: casos de estudio
Se realizó un análisis longitudinal (que incluyó datos retrospectivos y prospectivos) de la incidencia de crisis durante los 6 meses antes y después de la toma de la muestra en los 6 casos falsos positivos. Los resultados mostraron que: un paciente tuvo una crisis previa (5 meses antes de la toma de la muestra), 3 pacientes desarrollaron crisis dentro de los 3 meses posteriores a la toma de la muestra, 2 pacientes permanecieron en estado basal en todo el periodo analizado.
DISCUSIÓN
Caracterización de la muestra de evaluación
El test Chi-cuadrado muestra diferencias estadísticamente significativas en la distribución del estado clínico (estado basal vs CVO) entre las cohortes (χ²(1)=13,470; p<0.001), con un efecto moderado del tamaño de la muestra (φ=0.302; p<0,001). La cohorte de estimación del modelo contiene mayor proporción de pacientes en CVO (32.9% vs 8,3 % en la cohorte de evaluación), debido al diseño de los respectivos estudios. Las diferencias observadas, son consistentes con lo esperado dadas las características de cada estudio.
La comparación en cuanto al sexo revela que no hay diferencias estadísticamente significativas entre las cohortes y el efecto del tamaño de la muestra es despreciable (χ²(1)=0,729; p=0,393; φ=0,07; p=0,393). Para las variables continuas no se observan diferencias estadísticamente significativas, lo que verifica la similitud de las muestras estudiadas y soporta la robustez de los análisis subsecuentes.
Aplicación y optimización de la escala de riesgo
La representación gráfica de la distribución de los IR para cada categoría prueba una clara gradación del riesgo de CVO. Se observa una asociación significativa entre la clasificación clínica de complicaciones y el nivel de riesgo asignado (χ²(2)=32,727; p<0,001), manifestándose un patrón consistente: a mayor gravedad clínica, mayor probabilidad de pertenecer a la categoría de riesgo elevado. El grupo de pacientes sin complicaciones (estado basal) está compuesto por casos de riesgo menor (60,6 %) y moderado (30,3 %), mientras que el 9,1 % corresponde a riesgo mayor. Por el contrario, en los casos con CVO, el 100,0 % de los pacientes está clasificado como riesgo mayor, lo que demuestra la capacidad discriminatoria de la escala para identificar pacientes con evoluciones desfavorables para esta complicación.
Esta asociación es sólida y se corrobora mediante múltiples medidas estadísticas. Los coeficientes Phi y V de Cramer (0,674; p<0,001) indican una asociación muy marcada y significativa, mientras que las correlaciones de Pearson (r=0,554; p<0,001) y Spearman (ρ=0,486; p<0,001) confirman la existencia de un gradiente lineal positivo entre ambas variables. Estos resultados, consistentes a través de diversas métricas estadísticas, sustentan la utilidad del nivel de riesgo como un clasificador notable para la estratificación clínica y la toma de decisiones asistenciales.
Si bien la escala de tres categorías demuestra una adecuada capacidad discriminativa, el análisis de su implementación revela oportunidades de optimización. Desde la perspectiva metodológica, la subdivisión tripartita plantea desafíos en la precisión predictiva del instrumento. Asimismo, en términos de aplicabilidad clínica, la distinción entre riesgo menor y moderado muestra escasa relevancia práctica, dado que ambas categorías suelen tratarse con estrategias de seguimiento similares, sin que la subdivisión aporte valor añadido significativo a la toma de decisiones.
La teoría de decisión clínica respalda que la simplificación de instrumentos de evaluación puede reducir la complejidad operativa y optimizar la identificación de casos de alto riesgo, donde la acción clínica es más determinante.13 La escala dicotómica preserva la capacidad discriminatoria mientras mejora la eficiencia en la práctica clínica.14
La escala de riesgo simplificada demuestra una capacidad discriminativa entre pacientes que desarrollaron CVO y aquellos que se mantuvieron en estado basal excelente, el AUC de 0,957 es significativamente superior al valor de referencia aleatorio (0,5). Esta escala simplificada tiene una sensibilidad del 100,0 % y una especificidad del 90,9 %, lo que asegura la garantía en la detección global. El valor del 100,0 % del VPN confirma una correcta clasificación de los pacientes de bajo riesgo; y un VPP del 50,0 %. La interpretación clínica de los errores de clasificación se debe considerar de manera crítica. En este contexto, evitar falsos negativos tiene mayor prioridad que evitar falsos positivos, dada las consecuencias clínicas de omitir el seguimiento de un caso positivo real, que podría conllevar a una ausencia de tratamiento oportuno y la progresión de la condición médica.
Los falsos positivos introducen sobre-alerta en el sistema, pero representan un riesgo tratable y reversible tras una evaluación más exhaustiva. Por lo tanto, el rendimiento de esta escala está en correspondencia con el principio de precaución en la práctica clínica, donde las consecuencias de no actuar ante un caso verdadero positivo es mucho mayor que el de una intervención aparentemente innecesaria, ya que prioriza minimizar los falsos negativos, incluso a expensas de un número determinado de falsos positivos.
Un hallazgo clave es el punto de corte óptimo (2,055) según el índice de Youden, donde la escala muestra un desempeño global superior al punto de corte original (1,456), lo que mantiene la sensibilidad y VPN en 100,0 %, mientras mejora la especificidad, VPP, exactitud y F1-Score (Tabla 2). Dada la diferencia en el diseño del estudio y la prevalencia, se recomienda validar este ajuste en el punto de corte en poblaciones similares. Asimismo, se recomienda validar la escala de riesgo simplificada en una cohorte independiente, de ser posible en un estudio multicentro.
Los resultados demuestran que la escala de riesgo basada en marcadores redox (GSH y MDA) tiene un desempeño notable en la cohorte de evaluación. Estos hallazgos son compatibles con estudios previos que han explorado herramientas de estratificación en AF, aunque con diferencias metodológicas y poblacionales clave. Rincon EM15 desarrolló una escala para predecir infecciones bacterianas en niños con AF, lo que mostró un AUC de 0,86 (IC95%: 0,77--0,93), ligeramente inferior a los resultados del estudio. Esta diferencia podría atribuirse a que su modelo se centró en un tipo de complicación diferente (infecciones), mientras que esta escala evalúa el riesgo de CVO. Se prevé que el enfoque basado en el estado redox, supere estas limitaciones al capturar mecanismos fisiopatológicos compartidos por múltiples complicaciones. La función de los marcadores de estado redox es determinante en la fisiopatología de la mayoría de las complicaciones agudas, incluyendo las CVO.16
Evaluación prospectiva de los casos falsos positivos: casos de estudio
El análisis longitudinal de los casos falsos positivos revela hallazgos importantes sobre la naturaleza de estas clasificaciones. El paciente con una crisis previa a los 5 meses, fue considerado un falso positivo real, ya que la escala demuestra consistencia al clasificar como "riesgo menor" a otros cuatro pacientes con historiales de crisis similares. Este hallazgo confirma que la escala está efectivamente calibrada para evaluar el riesgo prospectivo y no el historial de eventos pasados, lo que valida su diseño como herramienta predictiva.
El hallazgo más significativo reside en que tres pacientes (50 % de los falsos positivos) desarrollaron una crisis dentro de los tres meses posteriores a la evaluación. Este resultado indica sólidamente que la escala puede anticipar un riesgo real en estos individuos. Por consiguiente, su clasificación inicial como de "riesgo mayor" pudiera no reflejar un error de clasificación del modelo, sino una subestimación de su capacidad predictiva; ya que podían considerarse verdaderos positivos con manifestación clínica retardada o en estado prodrómico. Esta capacidad de identificar riesgo antes de la manifestación clínica refuerza la utilidad clínica de la escala y justifica plenamente su alta sensibilidad. Más allá de tres meses la escala no tuvo valor predictivo.
Finalmente, los dos pacientes que permanecieron estables representan casos falsos positivos reales en el análisis longitudinal. El seguimiento de los falsos positivos indican que la escala posee un valor predictivo prospectivo, aunque debe incrementarse el número de casos estudiados para confirmar estos hallazgos. Estos resultados respaldan la hipótesis de que la alerta generada por determinado número de falsos positivos es clínicamente razonable, ya que involucra a pacientes con riesgo subyacente activo que pueden beneficiarse de un seguimiento más cercano.
Existe una base científica sólida para considerar que los niveles de MDA y GSH pueden ser indicadores del daño oxidativo en la AF,17,18 incluso antes de que las manifestaciones clínicas sean evidentes. Es conocido que la AF transcurre por un estado pro-oxidante crónico.19 La HbS es inherentemente inestable y se autooxida con mayor facilidad, lo que genera un exceso de ROS y el desequilibrio entre la producción de ROS y las defensas antioxidantes del organismo causa daño celular y contribuye a complicaciones como las crisis vaso-oclusivas.
El GSH es uno de los antioxidantes intracelulares más importantes y su depleción indica que el sistema de defensa está sobrepasado y prueba un agotamiento de las defensas antioxidantes incluso antes de una crisis.20 Por otro lado, el MDA es un producto final de la peroxidación lipídica y su elevación es un signo directo de daño oxidativo. La correlación de la alta concentración de este biomarcador con la gravedad de la enfermedad,20 indica que a mayor estrés oxidativo, más grave se manifiesta la enfermedad. Estas pruebas respaldan el hecho de que tanto GSH como MDA, pueden servir para evaluar el riesgo de complicaciones agudas en la AF.
Estas alteraciones bioquímicas preceden y se correlacionan con la aparición y gravedad de las manifestaciones clínicas, como las crisis vaso-oclusivas.18,19,20 Por lo tanto, el monitoreo de MDA y GSH es una herramienta valiosa para identificar de manera temprana a los pacientes con mayor riesgo de desarrollar CVO, lo que permiten intervenciones más oportunas y personalizadas. Los pacientes con un estrés oxidativo de base más elevado son más propensos a sufrir complicaciones, por lo que el monitoreo de estos biomarcadores puede identificar a los pacientes con mayor riesgo y evaluar la progresión de la enfermedad.
Limitaciones y perspectivas
El presente estudio tiene limitaciones que deben considerarse para interpretar adecuadamente los resultados. En primer lugar, en algunos casos, las historias clínicas incompletas limita la caracterización completa de los pacientes, lo que puede conllevar a subestimar el riesgo real de CVO. Asimismo, la generalización de las conclusiones puede verse limitada por el reducido tamaño muestral (n=72) y por las características específicas de la población estudiada en el Hospital Juan Bruno Zayas (como su perfil de comorbilidades y tratamientos). Por ello, se recomienda validar prospectivamente la escala de riesgo en estudios multicéntricos con cohortes más amplias y diversas, y ajustar los puntos de corte según el contexto clínico.
A pesar de estas limitaciones, este trabajo constituye una contribución a la evaluación del riesgo de CVO en la AF y la evaluación del paciente antes de la aparición de los síntomas. En los servicios de hematología del país no se cuenta con un instrumento clínico específico para la estratificación sistemática del riesgo de CVO y este estudio representa un primer paso para llenar ese vacío, lo que contribuye a individualizar el tratamiento del paciente de AF, aunque aún se requiere de mayor validación clínica.
Se concluye que la escala de riesgo basada en MDA y GSH muestra un desempeño excelente en esta cohorte de pacientes con anemia falciforme de Santiago de Cuba, lo que mostró una alta capacidad para discriminar entre pacientes con alto y bajo riesgo de crisis vaso-oclusivas. Su alto valor predictivo negativo la convierte en una herramienta potencialmente útil para la estratificación de riesgo en la práctica clínica.
REFERENCIAS BIBLIOGRÁFICAS
- Kato GJ, Piel FB, Reid CD, Gaston MH, Ohene Frempong K, Krishnamurti L, et al. Sickle cell disease. Nat Rev Dis Primers. 2018[citado: 16/10/2024]; 4(1):1-22. Disponible en: https://scispace.com/pdf/sickle-cell-disease-4naze3x8cu.pdf
- Sundd P, Gladwin MT, Novelli EM. Pathophysiology of sickle cell disease. Annu Rev Pathol. 2019[citado: 16/10/2024]; 14(1):263-92. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC7053558/
- Jang T, Poplawska M, Cimpeanu E, Mo G, Dutta D, Lim SH. Vaso-occlusive crisis in sickle cell disease: a vicious cycle of secondary events. J Transl Med. 2021[citado: 16/10/2024]; 19(1):1-11. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC8454100/
- Grupo nacional de hematología y bancos de sangre. Normas para el tratamiento de la drepanocitosis. Instituto Cubano de Hematología e Inmunología. Hematología. 2009 [citado: 16/10/2024]. Disponible en: https://especialidades.sld.cu/hematologia/hematopatias-tecnicas-y-servicios/derpanocitosis/programa-nacional-de-prevencion-de-anemia-falciforme/.
- Saah E, Fadaei P, Gurkan UA, Sheehan V. Sickle cell disease pathophysiology and related molecular and biophysical biomarkers. Hematol Oncol Clin North Am. 2022[citado: 16/10/2024]; 36(6):1077-95. Disponible en: https://www.sciencedirect.com/science/article/abs/pii/S0889858822000636?via%3Dihub .
- Higuera D, Hergueta E, Estepa N, Salazar E, Ibarra C, Pérez K, et al. Biomarcadores del estrés oxidativo y su asociación con la severidad clínica de pacientes venezolanos con síndrome drepanocítico. Invest Clin. 2019[citado: 16/10/2024]; 60(4):283-95. Disponible en: https://www.produccioncientificaluz.org/index.php/investigacion/article/view/31669/32916
- Cruz H, Alonso Y, Lores MA. Modelo predictivo de crisis vaso-oclusiva en la anemia drepanocítica. Rev Cubana Hematol Inmunol Hemoter. 2024[citado: 10/03/2025]; 40:e1819. Disponible en: https://revhematologia.sld.cu/index.php/hih/article/view/1819/1438 .
- Cruz H, Cala L, Ramos L, Roque C. Evaluación del desempeño de los métodos analíticos para el estado redox extracelular en suero humano. Rev Cubana Farm. 2021[citado 10/03/2025]; 54(3):1-14. Disponible en: https://revfarmacia.sld.cu/index.php/far/article/view/630/422
- Esterbauer H, Schaur R, Zollner H. Chemistry and Biochemistry of 4-Hydroxynonenal, Malondialdehyde and Related Aldehydes. Free Radic Biol Med. 1991[citado 10/03/2025]; 11(1):81-128. Disponible en: https://www.researchgate.net/publication/223737675_Chemistry_and_biochemistry_of_4-hydroxynonenal_malonaldehyde_and_related_aldehydes
- Erdelmeier I, Gérard MD, Yadan JC, Chaudière J. Reactions of N-methyl-2-phenylindole with malondialdehyde and 4-hydroxyalkenals. Mechanistic aspects of the colorimetric assay of lipid peroxidation. Chem Res Toxicol. 1998[citado 10/03/2025]; 11(10):1176-83. Disponible en: https://www.researchgate.net/publication/13508553_Reactions_of_1-Methyl-2-phenylindole_with_Malondialdehyde_and_4-Hydroxyalkenals_Analytical_Applications_to_a_Colorimetric_Assay_of_Lipid_Peroxidation
- StatsKingdom. Proportion confidence interval calculator. 2024[citado: 20/04/2025]. Disponible en: https://www.statskingdom.com/proportion-confidence-interval-calculator.html.
- Asociación Médica Mundial. Declaración de Helsinki: Principio éticos para las investigaciones médicas en seres humanos. 2024[citado: 11/03/2025]. Disponible en: https://www.wma.net/es/policies-post/declaracion-de-helsinki-de-la-amm-principios-eticos-para-las-investigaciones-medicas-en-seres-humanos/.
- Lifshitz A, García JL. Educación en Medicina. Enseñanza y aprendizaje de la clínica. Ciudad de México: Editorial Alfil; 2024[citado: 11/03/2025] Disponible en: https://www.researchgate.net/publication/275036076_Educacion_en_medicina_Ensenanza_y_aprendizaje_de_la_clinica
- Stefanini B, Tovoli F, Trevisani F, Marseglia M, Di Costanzo GG, Cabibbo G, et al. Prediction of cardiovascular risk in patients with hepatocellular carcinoma receiving anti-angiogenic drugs: lessons from sorafenib. Inter Emerg Med. 2024[citado: 11/03/2025]; 19(4):1151-60. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC11186950/
- Rincón López EM, Navarro Gómez ML, Hernández Sampelayo Matos T, Aguilera Alonso D, Dueñas Moreno E, Bellón Cano JM, et al. Risk-score based strategy to minimize antibiotic exposure in children with sickle cell disease and fever. Infection. 2022[citado: 11/03/2025]; 50(2):499-505. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC8484827/
- Vona R, Sposi NM, Mattia L, Gambardella L, Straface E, Pietraforte D. Sickle cell disease: role of oxidative stress and antioxidant therapy. Antioxidants. 2021[citado: 11/03/2025]; 10(2):296. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC7919654/
- Bahal M, Nyamati S, Hegde S, Kakkar A, Sood I, Kalra S. Estimation of Malondialdehyde Levels and Determination of Total Antioxidant Capacity in Serum and Saliva of Patient Affected with Sickle Cell Anemia. J Indian Acad Oral Med Radiol. 2022[citado: 11/03/2025]; 34(4):380-384. Disponible en: https://journals.lww.com/aomr/fulltext/2022/34040/estimation_of_malondialdehyde_levels_and.3.aspx
- Engwa GA, Okolie A, Chidili JP, Okore PA, Onu PC, Ugwu MO, et al. Relationship of oxidative stress and antioxidant response with vaso-occlusive crisis in sickle cell anaemia. Afr Health Sci. 2021[citado: 11/03/2025]; 21(1):150-8. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC8356617/
- Wang Q, Zennadi R. The role of RBC oxidative stress in sickle cell disease: from the molecular basis to pathologic implications. Antioxidants. 2021[citado: 11/03/2025]; 10(10):1608. Disponible en: https://www.mdpi.com/2076-3921/10/10/1608
- Jafri F, Seong G, Jang T, Cimpeanu E, Poplawska M, Dutta D, et al. L-glutamine for sickle cell disease: more than reducing redox. Ann Hematol. 2022[citado: 11/03/2025]; 101(8):1645-54. Disponible en: https://www.researchgate.net/publication/360607790_L-glutamine_for_sickle_cell_disease_more_than_reducing_redox
Conflicto de intereses
Los autores declaran que no hay conflicto de intereses.
Contribución de autoría
Yamirka Alonso Geli: Conceptualización, Curación de datos, Análisis formal, Investigación, Metodología, Administración del proyecto, Validación, Visualización, Redacción, Redacción-Revisión y edición 30 %.
Haydeé Cruz Vadell: Conceptualización, Curación de datos, Análisis formal, Investigación, Metodología, Administración del proyecto, Recursos, Supervisión, Validación, Visualización, Redacción, Redacción-Revisión y edición 20 %.
Lidia Suárez Beyríes: Curación de datos, Investigación, Recursos, Validación, Redacción-Revisión y edición 20 %.
Celeste Roque Rodríguez: Curación de datos, Investigación, Recursos, Redacción-Revisión y edición 15 %.
Manuel Arsenio Lores Guevara: Análisis formal, Investigación, Metodología, Administración del proyecto, Supervisión, Redacción-Revisión y edición 15 %.
Revisores: Dr. Carlos Olivers Cobian Caballero, Dra. Karima Maricel Gondres Legró
Corrector: Lic Alexander Brossard Taureaux